新股消息 | 映恩生物递表港交所 拥有由12款自主研发的ADC候选药物组成的管线
查投资获悉,据港交所8月26日披露,映恩生物(Duality Biotherapeutics, Inc.)向港交所主板提交上市申请,Morgan
Stanley、Jefferies、CITIC Securities为联席保荐人。

据招股书,映恩生物是抗体偶联药物(“ADC”)领域的全球领跑者,致力于为癌症和自身免疫性疾病等患者研发新一代ADC创新药物。公司利用自身的ADC技术平台,已建立起各种具有差异化的管线,公司正在推进这些管线,目标是革新癌症治疗模式,并提供可显著改善全球患者治疗效果的疗法。
据映恩生物介绍,自2019年成立以来,公司已建立由12款自主研发的ADC候选药物组成的极具创新及差异化的管线,包括:六款临床阶段ADC,在广泛未被满足临床需求的适应症中具有潜力,根据Frost & Sullivan,就总体或主要适应症的开发进展而言,每款均跻身全球领先之列;两款新一代双特异性ADC(“BsADC”)及一款治疗自身免疫性疾病的ADC(“自免ADC”)预计将于2024年至2026年进入临床阶段;多款其他临床前ADC。
在映恩生物六款临床阶段药物资产中,其中有五项已同时获得美国食品药品管理局(“FDA”)及中国国家药品监督管理局(“中国药监局”)的临床研究用新药(“IND”)批准。截至最后实际可行日期(2024年8月19日),公司在17个国家的230多个临床试验中心拥有七项全球多区域临床试验(“MRCT”),已有1000多名患者入组。公司的创新ADC资产已吸引全球领先的生物制药公司,并已建立数个全球合作伙伴关系,包括与BioNTech SE(“BioNTech”)、百济神州有限公司(“百济神州”)及 Adcendo ApS (“Adcendo”)的合作,交易总价值逾40亿美元。
此外,映恩生物的三项临床阶段资产(包括其的核心产品DB-1303/BNT323 及DB-1311/BNT324以及关键产品DB-1305/BNT325)已获得FDA的快速通道认定。DB-1303已获得FDA及中国药监局针对特定适应症授予的突破性疗法认定。
映恩生物还打造了四大领先ADC技术平台:映恩免疫毒素抗体偶联平台(DITAC)、映恩创新双特异性抗体偶联平台(DIBAC)、映恩免疫调节抗体偶联平台(DIMAC)及映恩独特有效载荷抗体偶联平台(DUPAC),以突破ADC治疗的边界。
映恩生物提到,截至最后实际可行日期,公司尚未获得任何候选药物的上市批准,亦未从产品销售中获得任何收入。预计公司的后期ADC将在未来几年实现商业化,映恩生物计划通过选择最佳商业模式(包括建立内部商业化能力及╱或与第三方(如分销商、合同销售组织(“CSO”)及许可合作伙伴)合作)使候选药物的商业价值最大化。
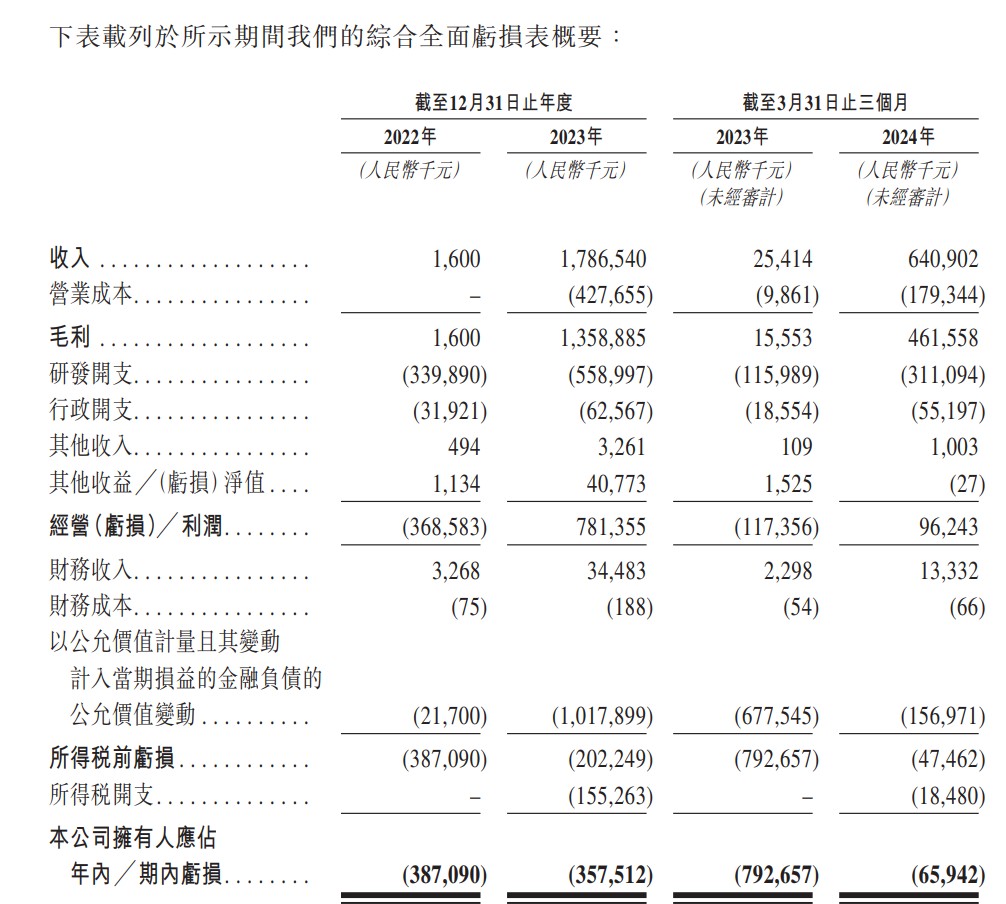
财务方面,于2022年、2023年、2024年截至3月31日止三个月,映恩生物的收入分别约为160万元、17.87亿元、6.41亿元人民币;期内亏损分别约为3.87亿元、3.58亿元、6594.2万元人民币。
据映恩生物在招股书中所述,公司在很大程度上倚赖其候选药物的成功。倘若公司未能就候选药物成功完成临床开发、取得监管批准或实现商业化,或倘公司的任何上述活动出现严重延误或成本超支,其业务及前景可能会受到重大不利影响。